近日,医学院曹轩教授团队在Journal of Nanobiotechnology(中科院一区Top期刊,IF:12.6,即时IF:14.9)发表题为《Engineered lipid hybrid nanoparticles for targeted delivery of SH2 superbinder and breast cancer therapy》的研究论文。
SH2超亲体蛋白(SH2S)是一种基于SH2结构域改造的工程多肽,其对酪氨酸磷酸化蛋白的结合能力显著增强,可用于多种癌症的诊断与治疗。然而,血清稳定性差、肿瘤靶向性不足等问题限制了其临床应用效果。
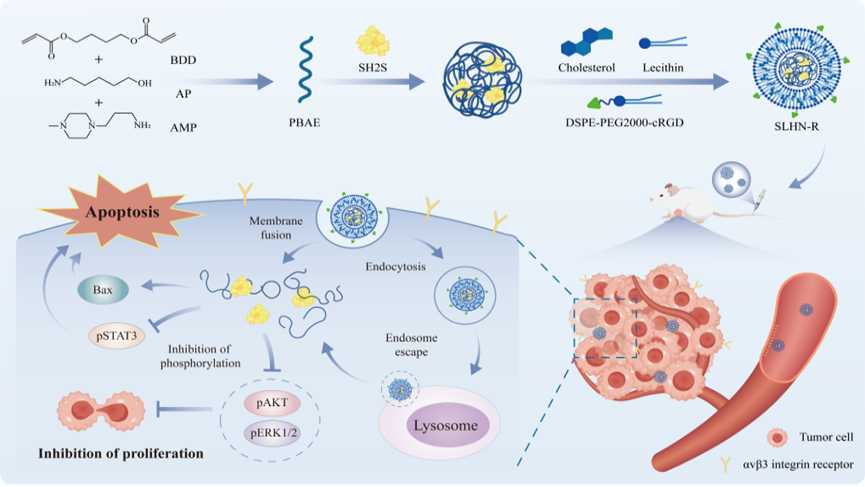
SLHN抗肿瘤模式图
为解决上述技术难题,本研究采用阳离子聚合物聚β-氨基酯、脂质及胆固醇,通过改良微流控技术构建了负载工程化SH2S的脂质杂化纳米粒(SLHN)。SLHN可通过膜融合与网格蛋白介导的内吞作用,将SH2S高效递送至肿瘤细胞内。进入细胞后,SLHN竞争性取代内源性含SH2结构域的蛋白,通过阻断AKT、ERK和STAT3的磷酸化,诱导肿瘤细胞凋亡并抑制其增殖。此外,经cRGD肽修饰的SLHN肿瘤靶向能力进一步提升,可在更低给药剂量下实现乳腺癌的高效治疗,且不良反应更温和。研究结果表明,SLHN在体内外均展现出良好的抗乳腺癌疗效,经cRGD主动靶向修饰后,其治疗效果进一步增强,该修饰策略丰富了脂质递送系统在抗癌蛋白递送中的应用,提升了SH2超亲体蛋白的临床应用价值。
联合培养研究生朱雨荷、桑亚洲、医学院青年教师杜琳娜为共同第一作者,医学院曹轩教授为该论文的倒数第一通讯作者,台州学院为第一单位,该研究得到了国家自然科学基金面上项目(81974468)支持。加拿大多伦多大学医学院Tony Pawson教授发现SH2结构域,开创性提出蛋白质模块化信号转导理论,系统阐明SH2结构域通过识别磷酸化酪氨酸介导蛋白相互作用,构建动态细胞信号网络的分子机制,这一发现改变了细胞信号转导、癌症研究和精准医疗等多个领域,推动了癌症靶向药物研发(如酪氨酸激酶抑制剂),获沃尔夫医学奖(2005)、京都奖(2008)、汤森路透引文桂冠奖(2012,诺贝尔生理学或医学奖提名)等国际殊荣。加拿大西安大略大学李顺成教授延续了Tony Pawson在SH2结构域方面的工作,并做了系统性拓展和创造性延伸。SH2超亲体蛋白是李顺成教授和曹轩教授等科研工作者共同持有的PCT国际发明专利,基于此专利技术成立的嘉华药锐科技(北京)有限公司专注于临床蛋白质组学技术研发,已经获得数亿元战略投资。
曹轩教授团队围绕SH2超亲体蛋白的抗肿瘤作用开展深入的研究,近几年以共同作者在Science signaling(Science子刊)、Nature Chemical Biology(Nature子刊),以通讯作者在ANAL CHIM ACTA(top期刊,IF:6)、JECCR(1区,IF:12.8)、CLIN TRANSL MED(1区,IF:10.6)、Cell Death & Disease(1区,IF:9.6)和Journal of Nanobiotechnology(1区,IF:12.6)发表一系列研究论文,以第三发明人获授权PCT国际专利1项,以第一发明人获授权中国发明专利3项。以上研究论文和发明专利为SH2超亲体蛋白抗肿瘤诊断与治疗产业化开发打下了坚实的基础。
论文链接为:https://link.springer.com/article/10.1186/s12951-026-04249-w